Mejore la posición de seguridad y conformidad a la vez que automatiza la conformidad con GxP mediante AWS.
En AWS, la seguridad y privacidad son la máxima prioridad
Obtenga más agilidad, mejore la seguridad de la información sanitaria personal y confidencial y automatice la conformidad con GxP mediante AWS.
La normativa de las GxP incluye los requisitos farmacéuticos internacionales subyacentes, como los que se establecen en la Ley Federal de Alimentos, Medicamentos y Cosméticos de EE. UU., la Ley del Servicio de Salud Pública de EE. UU., las normativas de la FDA, las directivas de la UE, las normativas de la MHRA del Reino Unido, las normativas japonesas o cualquier otra normativa o ley nacional aplicable que rija las operaciones de una empresa. Estas normativas incluyen, entre otras, las prácticas recomendadas de fabricación, prácticas recomendadas clínicas, prácticas recomendadas de laboratorio, prácticas recomendadas de calidad, prácticas recomendadas de farmacovigilancia, normativas sobre dispositivos médicos o la Ley de publicidad de medicamentos con prescripción.
Adquiera los controles de conformidad más exhaustivos con AWS, como la capacidad de cifrar a escala para cumplir con las leyes de privacidad nacionales, como PCI DSS, SOC, FedRAMP, NIST, ISO, HIPAA y HITRUST. AWS admite más estándares de seguridad y certificaciones de conformidad que ninguna otra oferta, lo que proporciona a las organizaciones de ciencias biológicas las herramientas, los servicios y la visibilidad necesarios para avanzar con más rapidez sin dejar a un lado la seguridad y la conformidad.
La creación de sistemas GxP en AWS permite tener un control mejorado sobre el entorno de TI, mejora la trazabilidad y la capacidad de llevar a cabo pruebas y ayuda a responder ante auditorías.
Descubra por qué las organizaciones de ciencias biológicas líderes, como Moderna y Bristol Myers Squibb, eligen AWS para ejecutar sus cargas de trabajo reguladas.
AWS y conformidad con las GxP
Con acceso a soluciones personalizadas, recursos técnicos y un equipo de expertos en GxP, AWS facilita a las organizaciones de ciencias biológicas que puedan migrar cargas de trabajo existentes y crear otras nuevas en la nube.
Diseñada para acelerar la migración de cargas de trabajo reguladas, la solución Conformidad con las GxP en AWS ayuda a las organizaciones a establecer un entorno alineado con las GxP que reduce los costos, mejora la seguridad y aumenta la agilidad.
Cómo admite AWS la conformidad con las GxP:
- Automatización del proceso de conformidad con las GxP: AWS proporciona las herramientas y la orientación necesarias para automatizar el proceso de conformidad de las GxP para que pueda desplazar con más velocidad a la vez que mantiene la conformidad. Más información
- Desarrollo de una infraestructura coherente y controlable: al aprovechar AWS para habilitar el entorno de GxP, puede crear plantillas que permiten utilizar la infraestructura en toda la organización con gran uniformidad. AWS también proporciona un control excelente sobre las personas que pueden modificar los elementos del software de la infraestructura, así como cuándo, dónde y cómo pueden hacerlo. Consulte cómo Merck configuró el control de sistemas GxP en la nube de AWS »
- Trazabilidad automática: use herramientas de AWS para registrar de forma automática una amplia variedad de actividades que tienen lugar en el entorno, entre las que se incluyen cómo se implementa la infraestructura y cómo se accede a ella y se configura. Esto mejora la trazabilidad en el entorno y facilita la respuesta ante solicitudes de auditoría. Más información
Recursos adicionales para crear aplicaciones de GxP en AWS:
Documento técnico
Consideraciones para usar productos de AWS en sistemas GxPDocumento técnico
Introducción a la auditoría del uso de AWSDocumento técnico
GxP en la nube de AWSInformación general
Security by Design
Privacidad de datos y AWS
Obtener la confianza de los clientes es la base de nuestro negocio en AWS. Nos ganamos esta confianza al trabajar para satisfacer las necesidades de privacidad de nuestros clientes y al ser transparentes en nuestros compromisos de privacidad.
Los clientes administran siempre el acceso a sus servicios y contenido. No obtenemos acceso ni utilizamos el contenido de los clientes para ningún fin sin el consentimiento del cliente. Con acceso a la infraestructura global más extensa, las organizaciones de ciencias biológicas pueden elegir las regiones en las que se almacenará su contenido. No migraremos ni replicaremos contenido del cliente fuera de las regiones que seleccione sin su consentimiento.
Responsabilidad compartida
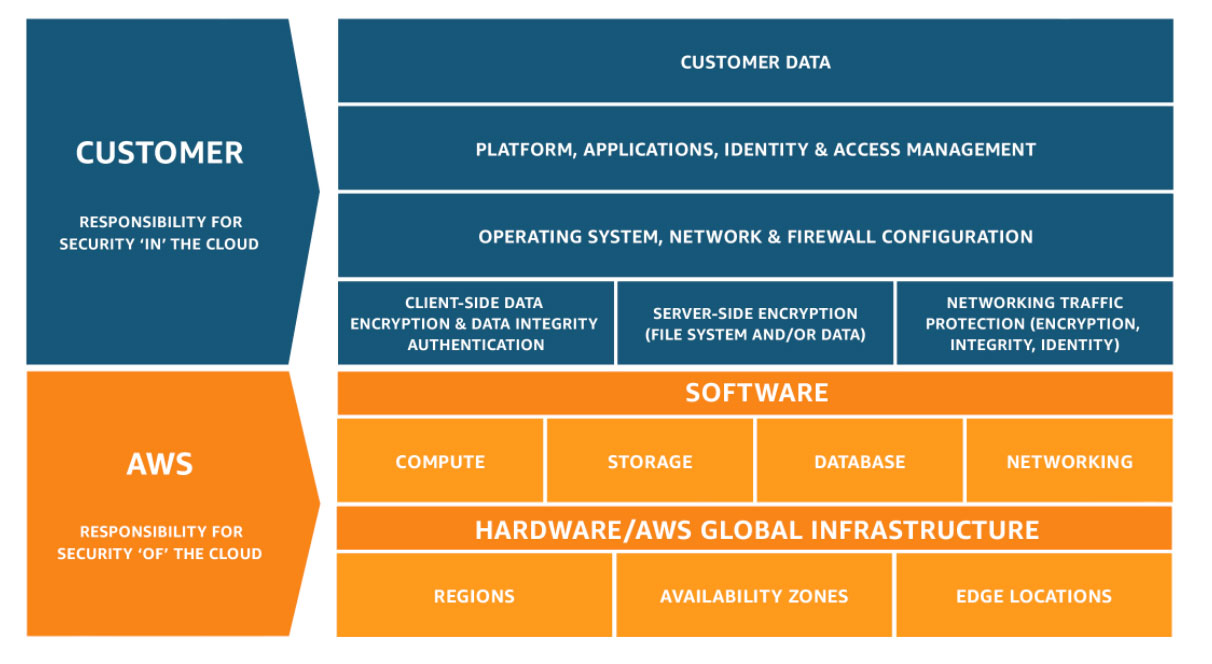
Los asuntos relacionados con la seguridad y la conformidad son una responsabilidad compartida entre AWS y el cliente. Este modelo compartido puede aliviar la carga operativa del cliente, ya que AWS opera, administra y controla los componentes del sistema operativo host y la capa de virtualización hasta la seguridad física de las instalaciones en las que funcionan los servicios.
Los clientes continúan siendo responsables de otros aspectos de la seguridad, como las medidas utilizadas para proteger las aplicaciones, que no difiere de los casos en los que las aplicaciones se ejecutan en centros de datos tradicionales.
Homologaciones y marcos reguladores de conformidad de ciencias biológicas de AWS
- Las certificaciones de conformidad de AWS demuestran la «seguridad de la nube» y la eficacia operativa de los controles de AWS. Los clientes son responsables de la seguridad en la nube.
- Los clientes heredan estas certificaciones de conformidad y pueden utilizarlas para demostrar parte de su conformidad a auditores y reguladores.
Un auditor independiente externo evalúa las certificaciones y acreditaciones de conformidad, lo cual tiene como resultado una certificación, un informe de auditoría o una acreditación de conformidad.
Los clientes de AWS tienen la responsabilidad de cumplir las leyes y regulaciones de conformidad correspondientes. En algunos casos, AWS ofrece funcionalidades (como las características de seguridad), recursos y acuerdos legales (como el acuerdo de procesamiento de datos y el anexo para socios empresariales de AWS) para respaldar los requisitos de conformidad del cliente.
Las homologaciones y los marcos reguladores de conformidad incluyen requisitos de seguridad y conformidad publicados para una finalidad específica, como un sector o una función determinados. AWS proporciona funcionalidades (como las características de seguridad) y recursos (incluidos manuales, documentos de comparación y documentos técnicos sobre conformidad) para estos tipos de programas.
Es importante mencionar el modelo de responsabilidad compartida cuando se habla de la conformidad normativa. AWS incorpora tecnologías de última generación, se adapta a las certificaciones y acreditaciones estándar del sector tanto a nivel global como local, cuando es posible, y se alinea con los marcos de cada sector para ayudar a facilitar una implementación adecuada de los servicios de AWS y cumplir los requisitos del sector sanitario. De acuerdo con el modelo de responsabilidad compartida, los clientes pueden heredar los controles y capacidades de conformidad para cumplir los requisitos de conformidad del sector sanitario en esa región.
La información que se encuentra a continuación muestra certificaciones representativas, leyes sanitarias y marcos relevantes.
Certificaciones y acreditaciones principales
ISO 9001
ISO 27001, 27017, 27018
SOC 1, 2, 3
Nivel 1 de PCI DSS
FedRAMP
Homologaciones y marcos principales
CSA (Cloud Security Alliance)
Escudo de Privacidad UE-EE. UU.
NIST
Controles de TI de BioPhorum
GxP
Estados Unidos

Estados Unidos (Regulador clave: FDA)
La Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) estableció la CFR 21 Parte 11 sobre registros electrónicos y firmas electrónicas. La CFR 21 Parte 11 se aplica a la industria de las ciencias biológicas que se incluyen en la Ley Federal de Alimentos, Medicamentos y Cosméticos de Estados Unidos, la Ley del Servicio de Salud Pública o cualquier otra normativa de la FDA que no sea la Parte 11. En conjunto, se identifican como "Reglas de predicado". En esencia, la Parte 11 se aplica cuando el registro en cuestión es predicado.
Más información:
- Data Integrity and Compliance With Drug CGMP Questions and Answers Guidance for Industry (Integridad de los datos y conformidad con la Guía de preguntas y respuestas sobre prácticas recomendadas de fabricación actuales de medicamentos para el sector industrial).
- Part 11, Electronic Records; Electronic Signatures - Scope and Application (Parte 11, registros electrónicos, firmas electrónicas: ámbito y aplicación)
- Sistemas GxP en AWS

Integridad de los datos y la FDA de los Estados Unidos:
Los reguladores de todo el mundo continúan investigando las preocupaciones y los problemas con la integridad de los datos en la industria de las ciencias biológicas. La FDA publicó una guía sobre la integridad de los datos como aclaración para las organizaciones de ciencias biológicas con el objetivo de corregir de forma proactiva las preocupaciones y los problemas en cuestión.
Reino Unido


Reino Unido (Regulador clave: MHRA)
La MHRA continúa centrándose cada vez más en la integridad de los datos. El aumento en el uso de captura de datos electrónicos, automatización de sistemas y tecnologías remotas ha aumentado a su vez la complejidad de las cadenas de suministro y los métodos de trabajo, que incluyen el uso de proveedores externos. La MHRA publicó una Guía de integridad de los datos específicamente para ofrecer más claridad y establecer las expectativas para la industria de las ciencias biológicas con el fin de garantizar la conformidad con la integridad de los datos.
Europa


Europa (Regulador clave: EMA): se aplica a los estados miembro de la Unión Europea
El Anexo 11 de la Unión Europea se aplica a cualquier forma de sistema informatizado como parte de las actividades reguladas de prácticas recomendadas de fabricación.

Integridad de los datos y la EMA:
La integridad de los datos continúa siendo un tema importante en todo el mundo. La EMA (Agencia Europea de Medicamentos) ha publicado una nueva guía de prácticas recomendadas de fabricación para garantizar la integridad de los datos que trata los datos relacionados con los que se generan en el proceso de prueba, fabricación, embalaje, distribución y supervisión de medicamentos.
Más información:
Historias destacadas de clientes

Lyell simplifica la validación de GxP en AWS, lo que redujo el tiempo de validación de la conformidad de semanas a minutos.

El entorno en la nube multiómico precisionFDA de la FDA, usa AWS para conectar datos y herramientas con expertos de todo el mundo para validar la tecnología de identificación de variantes.

Bristol Myers Squibb implementa una plataforma de autoservicio completamente automatizada para usuarios empresariales con gobernanza automatizada.

Merck reduce la duración de la evaluación de cambios hasta en un 90 % y el esfuerzo manual total por evaluación en un 30 a 70 %.
Introducción